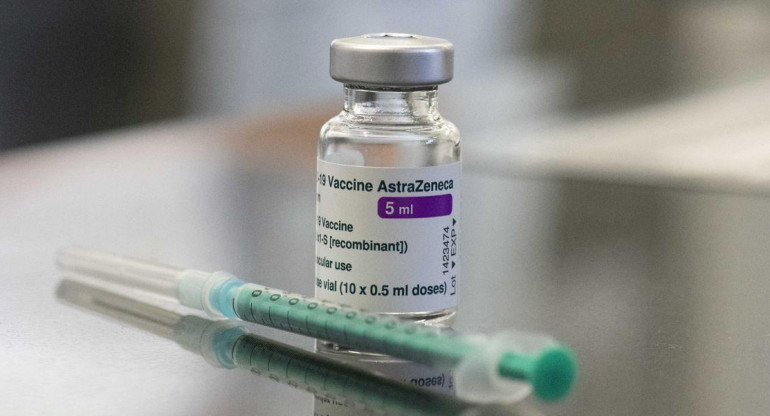
Comenzó este jueves en EE.UU. la audiencia pública de la FDA por vacuna de Pfizer y BioNTech contra el coronavirus
La Administración de Alimentos y Medicamentos (FDA) de Estados Unidos da los pasos finales para llegar a la autorización de la nueva vacuna contra el covid-19. La semana que viene, hará lo propio con la vacuna del laboratorio Moderna.
Por Canal26
Jueves 10 de Diciembre de 2020 - 10:27
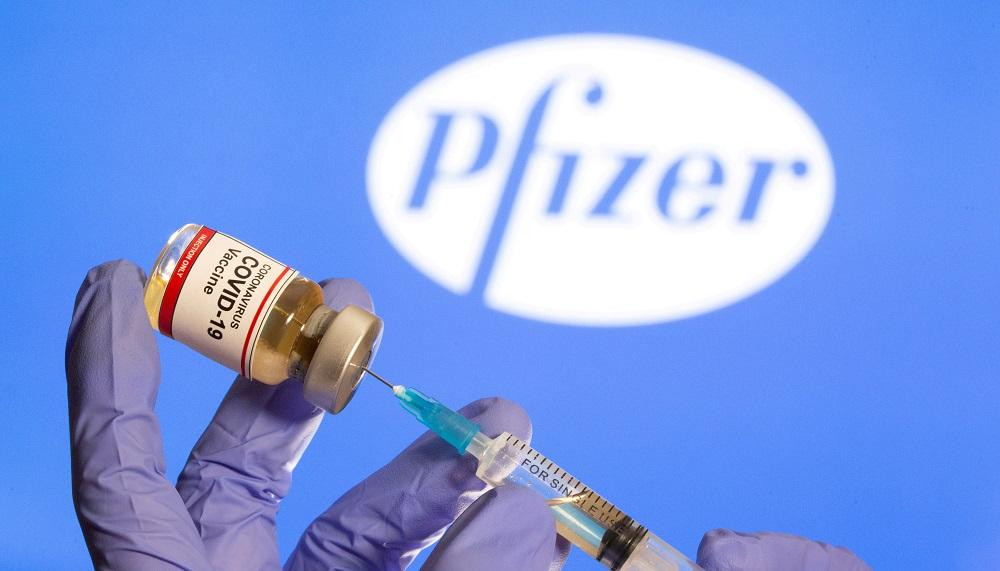 Vacuna de Pfizer contra el covid-19. Foto: Reuters.
Vacuna de Pfizer contra el covid-19. Foto: Reuters.
La Administración de Alimentos y Medicamentos (FDA) de Estados Unidos realizó este jueves la audiencia pública para definir la autorización de emergencia de la vacuna que fabrican Pfizer y BioNTech contra el coronavirus Covid- 19.
En tanto, la semana que viene, el jueves 17 de diciembre, será la audiencia para la autorización del uso emergencia de la vacuna que está fabricando Moderna.
La FDA publicó una crítica positiva para la vacuna de Pfizer y BioNTech pero todavía no está autorizado en Estados Unidos su aplicación de emergencia.
"Las presentaciones de la reunión se escucharán, verán, subtitularán y grabarán a través de una plataforma de teleconferencia en línea", anunció la FDA.
"El Comité Asesor de Vacunas y Productos Biológicos Relacionados (VRBPAC) del Centro de Evaluación e Investigación Biológica (CBER) se reunirá en sesión abierta para discutir la Autorización de Uso de Emergencia de la vacuna Pfizer-BioNTech COVID-19 para la prevención de COVID-19 en personas de 16 años o más", agregó.
Durante la audiencia de hoy se buscará responder las siguientes preguntas: ¿Cuánto protege la vacuna a personas de alto riesgo tales como los mayores de 65 años o los de cualquier edad con trastornos crónicos tales como obesidad o insuficiencia cardíaca?
-¿Se probó la vacuna en las comunidades negra, hispana y otras que sufrieron el embate de la pandemia para saber si es igualmente eficiente en esas poblaciones?
-¿Protege la vacuna contra la infección asintomática, o podrían estas personas, aunque vacunadas, seguir propagando inconscientemente el virus?
-¿Qué debe decirse a las mujeres embarazadas, ya que no fueron incluidas en el estudio de Pfizer?.
En tanto, la FDA también anunció la audiencia pública para la vacuna de Moderna, que será el jueves de la semana que viene.
"El 17 de diciembre de 2020, el Comité Asesor de Vacunas y Productos Biológicos Relacionados (VRBPAC) del Centro de Evaluación e Investigación Biológica (CBER) se reunirá en sesión abierta para discutir la Autorización de Uso de Emergencia de Moderna, Inc., COVID-19 Vacuna para la prevención de COVID-19 en personas mayores de 18 años", anunció la FDA.
Más Leídas
-
1
Rusia recubre sus aviones militares con neumáticos para defenderse de los drones ucranianos

-
2
Trump lamentó que Irán no firmara el acuerdo nuclear y advirtió que "todo el mundo debería evacuar Teherán inmediatamente"

-
3
¿Cerca de una Tercera Guerra Mundial?: un prestigioso informe advirtió sobre el riesgo de una nueva carrera de armas nucleares

-
4
La princesa Leonor y su camino hacia la Corona: cómo entrena y en qué disciplinas se forma la futura reina de España

-
5
Listos para la Tercera Guerra Mundial: China y Rusia invirtieron en una tecnología militar que preocupa a Estados Unidos